Centro Médico de Caracas. Hospital Universitario de Caracas
La neuralgia del trigémino se define, por la IASP (International Association for the Study of Pain), como “dolor paroxístico, unilateral, severo, penetrante, de corta duración, recurrente, en la distribución de una o varias de las ramas del V nervio craneal”. Puede ser esencial o sintomática, secundaria a esclerosis múltiple o lesiones tumorales en el ángulo pontocerebeloso, la prevalencia es del 0,1% de la población. Método: Se trataron 46 pacientes mediante la técnica de microcompresión percutánea del ganglio de Gasser con balón de Fogarty (Técnica de Mullan). Resultados: Se realizó el procedimiento en 46 pacientes con neuralgia del trigémino (N = 46). La edad varió desde los 28 hasta los 78 años con una media de 62 años. Sexo femenino en 28 casos (60,9%) y 18 pacientes masculinos (39,1%). Lado derecho en 26 pacientes (56,5%) e izquierdo en 20 (43,5%). En 43 pacientes la desaparición del dolor fue inmediata al terminar el procedimiento, dos pacientes presentaron dolor post-operatorio uno con desaparición del mismo en menos de 24 horas y uno con persistencia del dolor que ameritó realizarse una descompresiva microvascular por fosa posterior. Conclusión La técnica de microcompresión percutánea del ganglio de Gasser, demuestra ser un método efectivo, con resultados comparables con las estadísticas internacionales. RCM 2015; 143(2):19-32
Palabras clave: Neuralgia del Trigémino. Dolor facial. Microcompresión percutánea. Ganglio de Gasser. Técnica de Mullan. Balón de Fogarty.
Trigeminal neuralgia is defined by the IASP (International Association for the Study of Pain), as “Paroxistic pain, unilateral, severe, sharp, short, appellant, in the distribution of one or more branches of the V cranial nerve “. It can be idiopathic or secondary to multiple sclerosis or symptomatic to tumor lesions in the cerebellopontine angle, the prevalence is 0.1% of the population. Method: 46 patients were treated by percutaneous microcompression Gasser ganglion Fogarty balloon (Mullan technique). Results: The procedure was performed in 46 patients with trigeminal neuralgia (N = 46). Ages ranged from 28 to 78 years with a mean of 62 years. Female in 28 cases (60.9%) and 18 male patients (39.1%). Right side in 26 patients (56.5%) and left in 20 (43.5%). In 43 patients the disappearance of pain was immediate upon completion of the procedure, two patients had postoperative pain disappearance, of this, one in less than 24 hours and one with persistent pain that required microvascular decompression performed by posterior fossa. Conclusion: The percutaneous microcompression Gasser ganglion, proves to be an effective method, with results comparable to international statistics.. RCM 2015; 143(2):19-32
Key words: Trigeminal Neuralgia. Facial pain. Percutaneous Microcompression. Ganglion Gasser. Mullan technique. Fogarty balloon.
Aliviar el dolor ha sido desde siempre uno de los anhelos y motivaciones que han impulsado el desarrollo de la medicina y en especial cuando se trata de la nuralgia del trigémino, dolor de extrema intensidad, que puede llevar al paciente a tal desesperanza, que incluso puede decidir su autolisis.
La neuralgia del trigémino se define, por la IASP (International Association for the Study of Pain), como “dolor paroxístico, unilateral, severo, penetrante, de corta duración, recurrente, en la distribución de una o varias de las ramas del V nervio craneal”. Puede ser esencial o sintomática, secundaria a esclerosis múltiple o lesiones tumorales en el ángulo pontocerebeloso, la prevalencia es del 0,1% de la población. (1)
Lo extremo del dolor y lo refractario muchas veces al tratamiento farmacológico, han impulsado a la postulación de diversas teorías, tanto para explicar su etiología, así como el intento de desarrollo de múltiples procedimientos y técnicas a lo largo de la historia para aliviar tan severo padecimiento.
En 1983, aparece como alternativa descrita por Mullan y Lichtor, la microcompresión percutánea del ganglio de Gasser con balón de Fogarty. Se trata de introducir un balón de Fogarty de embolectomía en el ganglio de Gasser para producir isquemia selectiva de esta estructura anatómica con el consecuente alivio del dolor. Es un procedimiento realizado bajo anestesia general, con resultados inmediatos, no requiere de la disposición de grandes tecnologías y con mínima morbilidad. (2)
El objetivo básico del presente trabajo es describir la técnica de la microcompresión percutánea del ganglio de Gasser con balón de Fogarty (técnica de Mullan) para el tratamiento de la neuralgia del trigémino, mostrar los resultados obtenidos en la serie de los casos tratados y lograr la difusión de dicho procedimiento en beneficio de nuestros pacientes.
Antecedentes históricos de los procedimientos quirúrgicos para el tratamiento de la neuralgia del trigémino:
Los intentos iniciales para el tratamiento quirúrgico de la neuralgia del trigémino iban orientados a realizar secciones o ablaciones de las ramas nerviosas periféricas de este par craneal. Este tipo de procedimientos ya fueron probablemente propuestos por Albinus y Galeno y a comienzos del siglo XVIII cirujanos como Schilichting y Maréchal, médico y cirujano personal de Luis XIV. En múltiples artículos se le atribuye a Avicenna (980-1036), médico y filósofo Persa, la descripción de la neuralgia del trigémino. En su libro Qanum, desórdenes de la cara y los dientes, habla de dolor facial con espasmos. (3)
Según Lewy, hay un error importante que se ha copiado una y otra vez. Es la creencia de que la escuela de medicina árabe poseía conocimientos de la neuralgia del trigémino. Esto es principalmente el resultado de una mala interpretación de una traducción equívoca latina del texto árabe. La entidad en cuestión era más probable parálisis facial (4).
Jurjani (1066-1136) describe el cuadro de dolor hemifacial que afecta la mandíbula con espasmo y mucha ansiedad. (3)
Una de las primeras descripciones claras de la neuralgia del trigémino fue la de John Locke en 1677, en la esposa del embajador Británico en Francia. Pero fue Nicholas André en 1756 quien describe la enfermedad en un grupo de pacientes en su libro “Observations pratiques sur les maladies de l´urethre et sur plusieurs faits”. Tras 318 páginas dedicadas a enfermedades de la uretra, la mayoría de origen venéreo, inicia bajo el título de “Remarques sur certains mouvements convulsivs” una detallada descripción de cinco pacientes con dolor facial paroxístico. El primero de ellos lo vio en 1732. Se trataba de una mujer a la que habían realizado la extracción de tres dientes en la arcada dentaria superior en un intento de curar la formación continua de un absceso a este nivel. Las extracciones fueron efectivas en la mejora de la infección pero dejaron a la paciente con unos dolores paroxísticos, muy intensos, de corta duración y que se podían provocar. Además iban acompañados de marcadas y características muecas de dolor. (4)
En 1730 Maréchal había fracasado en su intento de seccionar el nervio infraorbitario. André propuso dos años después aplicar piedras cáusticas y líquido cáustico durante 10 o 12 días hasta que el nervio infraorbitario fuese destruido. La paciente mejoró completamente de su dolor y ante una nueva recaída 18 meses después fue de nuevo tratada y definitivamente curada.(4)
A esta enfermedad que cursaba con “estos movimientos violentos” André la denominó “tic douloureux”. Reconoció que se trataba de una entidad diferente a las otras y, a pesar del carácter explosivo de los episodios, “no se podía denominar propiamente convulsión... dado que los movimientos no son involuntarios”. (5)
En 1787, Pujol y otros cirujanos franceses y europeos de la época reconocieron la enfermedad con la denominación otorgada previamente por André, y sugirieron que más de un nervio de la cara debía ser seccionado (en ocasiones no bastaba con el nervio infraorbitario), y con frecuencia se seccionaba el nervio facial también (nervio motor de la cara). Pujol ya predijo que las extracciones dentarias eran inefectivas en el tratamiento de este dolor. (3)
A comienzos del siglo XIX, Sir Charles Bell realizó la distinción entre el papel motor del nervio facial y el papel sensitivo del nervio trigémino. Aún así cirujanos de la época, incluido su propio hermano, John Bell, continuaron seccionando el nervio facial para el tratamiento del “tic douloureux”. (6)
En 1843, Malgaigne cortó la segunda división del nervio 2 cm. posterior al borde inferior de la órbita, rompiendo el suelo de la órbita, y después tirando del nervio a través del foramen infraorbitario. El objetivo era retrasar la regeneración del nervio seccionándolo a un nivel más posterior. (4)
Todas estas técnicas de neurectomía no eran realmente efectivas, y a mediados y finales del siglo XIX aparecen artículos reflejando el bajo número de curaciones, solo 18 casos de 100, descrito por Rose en 1892, así como la alta incidencia de trastornos sensitivos en forma de hipoestesias y alodinias.(4)
Por todo esto, aparecen técnicas de gangliectomía, sección del ganglio de Gasser, situado en el cavum de Meckel sobre la fosita de Rossenmüller, que es una depresión en la porción medial y posterior de la fosa media. (4)
El primero en llevarla a cabo fue el cirujano inglés William Rose en 1890. Su técnica suponía el acceso y sección del ganglio a través de la base del cráneo realizando un trépano, al lado del foramen ovale. (4)
En 1891 Hartley modificó el acceso y detalló la facilidad que suponía ir directamente lateral al ganglio, através de la escama del hueso temporal, levantando la duramadre (capa que cubre al cerebro). El abordaje de Hartley-Krause fue perfeccionado por Tyffany en 1896 quien propone seccionar aquella parte del ganglio encargada de la segunda y tercera división, dado observó que la sección de la primera rama iba asociada a anestesia corneal con los problemas de queratitis y úlcera corneal que ello comportaba. Estas cirugías iban asociadas a una alta mortalidad que podía llegar al 24% según las series de Tyffany. Fue Cushing en 1900 quien consigue reducir de manera notable la mortalidad a 2 casos de 332 pacientes. Esto se consiguió gracias a los estudios en 30 cadáveres, y a las “precauciones” anestésicas que seguía Cushing en sus cirugías. (7)
La alta mortalidad de las gangliectomías llevó a diseñar las rizotomías. Horsley en 1891 describió la sección a nivel de la protuberancia de las raíces que conformaban el ganglio de Gasser. En esta primera rizotomía el paciente falleció debido a un “shock”, a pesar según Horsley, de lo bien que transcurría la cirugía. El abordaje fue intradural con elevación del lóbulo temporal. Posteriormente, Spiller y Frazier popularizaron en 1901 la rizotomía siguiendo un abordaje extradural. La cirugía se extendió hasta mediados del siglo pasado, pero seguían apareciendo complicaciones como son: la parálisis facial por edema causado por la tracción que ejerce el nervio petroso superficial mayor sobre el ganglio geniculado del facial, al elevar extraduralmente el lóbulo temporal. También se siguieron viendo casos de anestesia dolorosa, disestesias y anestesia corneal. (8)
A partir de 1925 el neurocirujano norteamericano Walter Dandy comenzó a preconizar el abordaje a la raíz del nervio por la fosa posterior. Observó que en numerosas ocasiones el nervio presentaba indentaciones por vasos sanguíneos. Recomendaba para esos casos la separación de los vasos, pero sobretodo una rizotomía parcial, con la que conseguía preservar la sensibilidad de la hemicara y curar el dolor. El problema de este tipo de cirugía era el considerable número de recurrencias, y la mortalidad asociada al abordaje por vía posterior, hasta 8 veces mayor que por la fosa media en la serie de Olivecrona, por lo que no se popularizó este abordaje hasta comienzos de la segunda mitad del siglo pasado. (8)
En 1950 Gardner y Milkos describieron el beneficio que suponía la descompresión vascular del nervio para el tratamiento de la neuralgia del V par craneal. En los años 70, Jannetta perfeccionó la técnica y confirmó que el dolor se podía solucionar con la liberación del nervio de los vasos que lo comprimían, sin necesidad de seccionar el nervio. (9)
La radiocirugía se desarrolló primero en el Instituto Karolinska de Estocolmo, Suecia, en 1949 conjuntamente por el Dr. Lars Leksell, un neurocirujano y Bjorn Larsson, un radiólogo de la Universidad de Uppsala. En 1968, desarrollaron el bisturí de rayos gamma (Gamma-knife), un nuevo dispositivo en exclusiva para la radiocirugía, que consistía de las fuentes radiactivas de Cobalto-60 colocado en una especie de casco con los canales centrales para la irradiación, usando rayos gamma para ser dirigidos al ganglio de Gasser. (10)
La termocoagulación percutánea fué ideada por Sweet et al en 1974 (11). Basada en la electrocoagulación realizada por Kirschner (12), consiste en destruir las fibras amielínicas transmisoras del dolor a nivel retrogasseriano mediante temperatura que se alcanza en la punta de un electrodo introducido a través del foramen oval. (11)
En 1980 se empieza a usar el acelerador lineal (LINAC) para radiocirugía, siendo pionera la Universidad de la Florida College of Medicine y presentado por Betti y Colombo a mediados de 1980, entre sus indicaciones se encuentra el tratamiento de la neuralgia del trigémino, irradiando la emergencia de la raíz del V nervio craneal afectado. (13,14)
La inyección retrogasseriana de glicerol fue introducida por Hakanson en 1981, consiste en introducir este producto mediante punción percutánea, a través del foramen oval mediante control radiológico con contraste. (15)
En 1983 la microcompresión percutánea del ganglio de Gasser con balón de Fogarty aparece como alternativa descrita por por Mullan y Lichtor. Se trata de introducir un balón de Fogarty de embolectomía en el ganglio de Gasser siguiendo una técnica similar a la descrita para los procedimientos de radiofrecuencia para la entrada al ganglio de Gasser. La aguja por la que se introduce el catéter es bastante más gruesa. Procedimiento realizado bajo anestesia general con buenos resultados y mínima morbilidad (2). Procedimiento que motiva el presente trabajo.
En Venezuela diferentes autores y especialistas se han ocupado del tema, pero pocos lo han comunicado a la literatura.
Vale mencionar al Dr. Roberto Lucca quien recopila diez años de experiencia de bloqueos terapéuticos en el departamento de anestesia del hospital privado Centro Médico de Caracas en 1967 llegando a la fosa de Gasser con referencias anatómicas sin fluoroscopia, con 279 procedimientos en 60 pacientes. (16)
El Dr. Abraham Krivoy incursionó en varias técnicas para el tratamiento de la neuralgia del trigémino, experiencia que se resume en el Consenso Venezolano del Dolor Neuropático. (17) En 1971 reporta la primera rizotomía transtentorial del trigémino bajo microscopio realizada en el Hospital Universitario de Caracas el 18-03-71. Practica la neurectomía subtemporal del ganglio de Gasser, técnica de Frazier y la descompresiva vascular de fosa posterior, técnica de Janetta. (17, 18,19)
El Dr. Rafael Galera acumuló experiencia en la rizotomía con glicerol presentando buenos resultados. (20)
En 1978 el Dr. Ernesto Carvallo Isturiz se desarrolló en el campo de la rizotomía percutánea mediante radiofrecuencia con resultados comparables con experiencias en centros a nivel internacional. (17, 20, 21)
El Dr. Antonio Daher en la ciudad de Valencia reporta 100 casos de tratamiento de neuralgia del trigémino mediante la técnica de descompresiva microvascular de Janetta con excelentes resultados. (22)
El Dr. Salvador Somaza en el 2004 presenta sus primeros dos casos de tratamiento de la neuralgia del trigémino mediante radiocirugía con acelerador lineal. (23)
El dolor a través del ganglio de Gasser se conduce por distintos tipos de fibras nerviosas, entre ellas las fibras A delta y las fibras C. La primera son mielinizadas, más gruesas, lo que las hace más sensibles a la isquemia mientras que la fibras C son más delgadas y más resistentes a factor compresión. La conducción del dolor en la neuralgia del trigémino, a través del ganglio de Gasser se realiza básicamente por las fibras A delta. La microcompresión percutánea del ganglio de Gasser busca destruir por medio presión mecánica, que a su vez conduce a isquemia, las fibras nociceptivas milinizadas A-delta por donde viaja el impulso de la neuralgia del trigémino, preservando otros tipos de fibras. (Fig 1) Es una forma parcialmente selectiva de lisis siempre y cuando no se sobrepase el tiempo de compresión a lo estipulado. (2, 24, 25, 26)
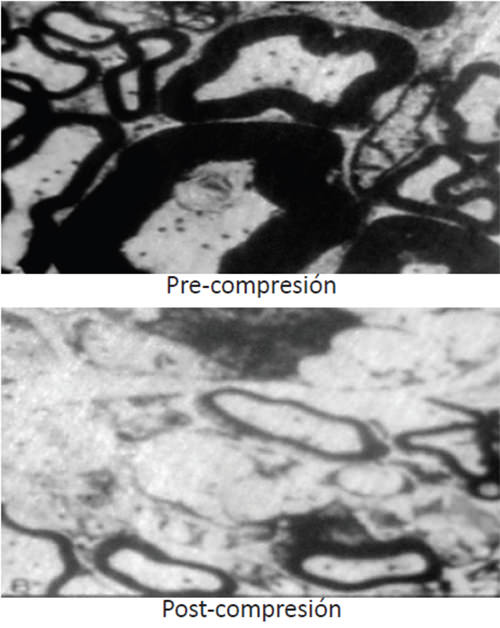
La técnica se realiza en quirófano bajo anestesia general balanceada con monitorización continua, en especial, de la frecuencia cardíaca y la tensión arterial.
Con el paciente en decúbito supino, la cabeza debe estar en hiperextensión, ligeramente girada, unos 25 grados, hacia el lado contrario al lado del dolor, con el equipo de rayos en proyección anteroposterior o ligeramente caudo-craneal hasta observar el foramen oval por dentro de la línea de la articulación témporomandibular. (Fig. 2)
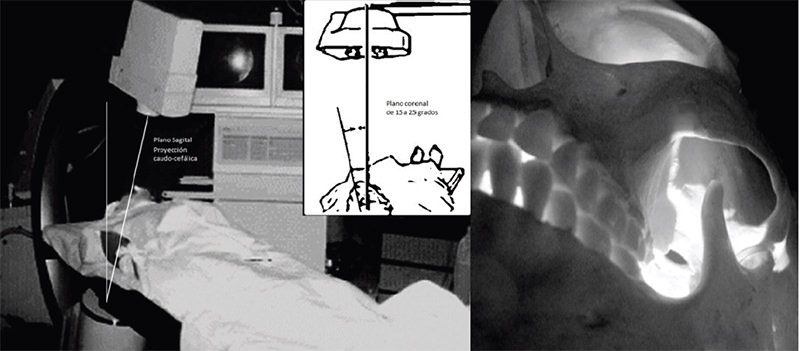
Previa antisepsia, se marca el punto de entrada sobre la piel, se encuentra a dos centímetro y medio lateral a la comisura labial. (Fig 3) Así como, se marcan dos referencias externas a dirigir la aguja en su trayecto de entrada hacia el agujero oval. El primero, la línea medio pupilar en el plano coronal y el segundo punto, la unión de los dos tercios anteriores con el tercio posterior de una línea que va del canto externo del ojo al meato auditivo externo, para la guía de la aguja en el plano sagital.
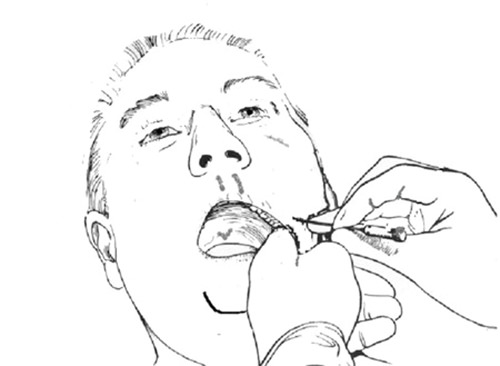
Se completa la colocación de campos, se incinde la piel de manera puntiforme con bisturí 11, se introduce el trocar seleccionado (Nº11g) y se lleva al agujero oval guiado tanto por las referencias externas como por fluoroscopia. (Fig. 4) Al llegar al agujero oval se evidencian cambios hemodinámicos importantes como bradicardia e hipertensión.
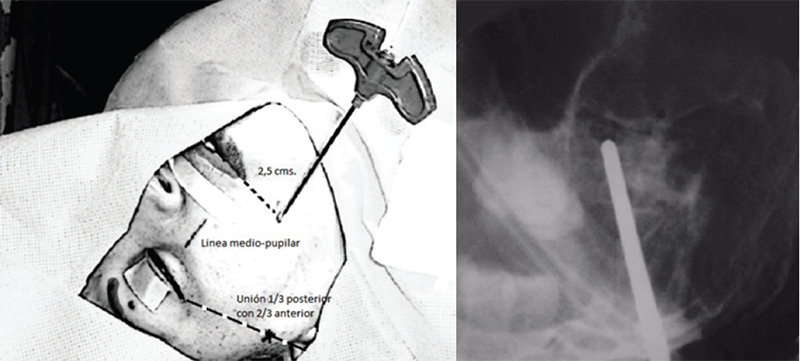
El uso de atropina puede estar indicado. Una vez que se ha penetrado por el agujero oval, se cambia la proyección del rayo a una vista lateral para ver la silla turca, el seno esfenoidal y el plano del clivus. El ángulo que se forma entre el clivus y la cara anterior del peñasco confirma que la dirección de la aguja es adecuada. Acto seguido pasamos un guiador de Seldinger para iniciar y facilitar el paso del catéter de Fogarty 4F, cuyo balón debe ser probado previo al inicio del procedimiento. (Fig. 5)
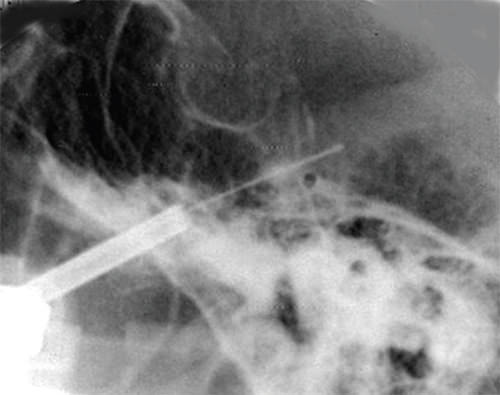
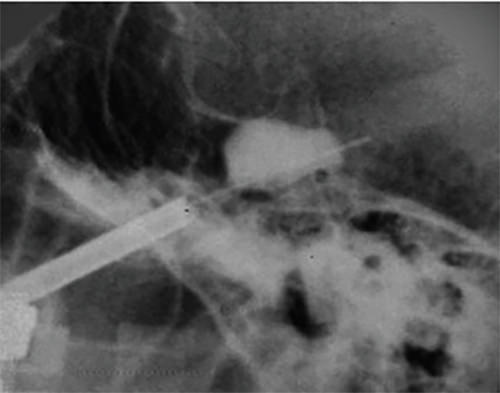
Se introduce el catéter de Forgarty y se avanza 10mm por encima del plano óseo para posicionarlo en el cavum de Meckel. Se insufla el balón con medio de contraste hidrosoluble con un volumen aproximado de 0,75 a 1 cc. Si el balón adquiere la forma característica, en “pera” (Fig. 6), que indica que su posición es adecuada, se mantiene inflado por un período de uno a dos minutos seguido de su vaciado. Se procede al inmediato retiro del trocar en conjunto con el catéter para evitar que este sea cortado por el bisel de la aguja. Una vez retirado el trocar, se realiza compresión hacia la zona pterigo-maxilar por unos minutos y se coloca una pequeña cura en el punto de entrada de la piel.
En el Hospital Universitario de Caracas y en el Centro Médico de Caracas, durante el período comprendido entre 1994 y mayo de 2003 se seleccionaron 46 pacientes con diagnóstico de neuralgia del trigémino, refractaria al manejo farmacológico en quienes se realizó la técnica de microcompresión percutánea del ganglio de Gasser, con un seguimiento en el postoperatorio no inferior a diez años.
Se incluyeron aquellos pacientes con criterios clínicos de neuralgia del trigémino clásica, con imagenología que demostró la ausencia de otra patología, con antecedente de fracaso en la terapia farmacológica, ausencia de enfermedades concomitantes o medicación crónica que contraindicaran la realización del procedimiento, y la autorización verbal del paciente posterior a una amplia explicación del procedimiento
En vista de que, desde el punto de vista de las cualidades del dolor de la neuralgia del trigémino clásica se caracteriza por ser de tipo paroxístico, la evaluación de los resultados posteriores al procedimiento terapéutico se hizo en base a presencia o ausencia de dicho dolor, sin la necesidad de incluir escalas intermedias.
Se realizó el procedimiento en 46 pacientes con neuralgia del trigémino (N = 46) de los cuales el primero fue en una neuralgia post-herpética de la primera rama del trigémino y los siguientes 45 en neuralgia del trigémino típica.
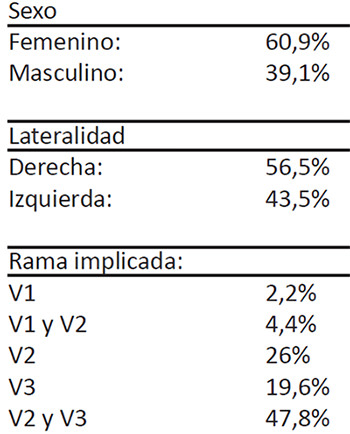
La edad varió desde los 28 hasta los 78 años con una media de 62 años. Sexo femenino en 28 casos (60,9%) y 18 pacientes masculinos (39,1%). Lado derecho en 26 pacientes (56,5%) e izquierdo en 20 (43,5%). Un caso de la primera rama (2,2%), 2 casos de la primera y segunda rama (4,4%), 12 casos de la segunda rama (26%), 9 casos de la tercera rama (19,6%) y 22 casos de la segunda y tercera rama (47,8%). (Tabla 1)
En 43 pacientes (93%) la desaparición del dolor fue inmediata al terminar el procedimiento.
Dos (4%) pacientes presentaron dolor post-operatorio uno con desaparición del mismo en menos de 24 horas espontáneamente, y otro con persistencia del dolor que ameritó realizar un procedimiento de descompresiva microvascular por fosa posterior en un segundo tiempo.
El primer paciente realizado, presentaba diagnóstico de neuralgia post-herpética, si bien no se trató de una neuralgia clásica, tenía componentes paroxísticos dentro de su cuadro doloroso tan severos y refractarios que motivó iniciar la implementación de esta técnica. Este paciente presentó una mejora significativa por desaparición del dolor paroxístico con persistencia de dolor de fondo de menor intensidad.
En 34 pacientes (74%), se retiró la medicación previa al tratamiento quirúrgico en un lapso de una semana.
El en lapso de seguimiento de 10 años, se presentó recidiva en 8 casos (17,4%), de los cuales se repitió el procedimiento en 4 de ellos, con mejora nuevamente de del dolor en los 4 casos.
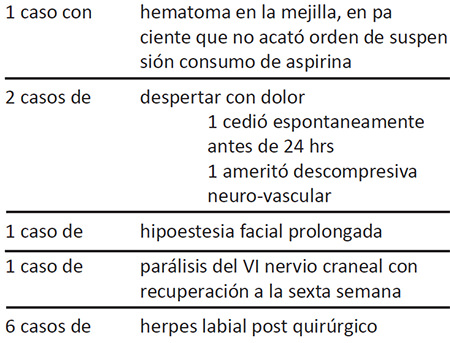
Entre las complicaciones observadas, en todos los pacientes se presentó algún grado de disestesia leve no mayor de 1 semana que no los incomodaba. La debilidad de masetero no fue significativa, no fue reportada espontáneamente por los pacientes sino una vez interrogado se evidenció en el 50 % de los pacientes. No hubo anestesia dolorosa ni pérdida del reflejo corneal. No hubo mortalidad. Otras complicaciones se resumen en la Tabla 2.
La neuralgia del trigémino se define, por la IASP (International Association for the Study of Pain), como “dolor paroxístico, unilateral, severo, penetrante, de corta duración, recurrente, en la distribución de una o varias de las ramas del V nervio craneal”. Puede ser esencial o sintomática, secundaria a esclerosis múltiple o lesiones tumorales en el ángulo pontocerebeloso (1).
Diversos estudios han estimado la prevalencia de la neuralgia del trigémino, según los mismos, la prevalencia es del 0,1% de la población. Algunos muestran una incidencia anual de 5,9/100.000 mujeres y 3,4/100.000 hombres (Clínica Mayo). Un 10% de todos los casos tratados con esta clínica se debieron a tumores (27).
Etiológicamente, entre las teorías más aceptadas, la neuralgia esencial del trigémino se asocia a un cuadro de dolor neuropático secundario a la compresión de tipo vascular de la zona de entrada del nervio en el tronco cerebral. Generalmente esta compresión es producida por vasos sanguíneos principalmente ramas de las arterias cerebelosas o venas de drenaje o menos frecuente por tumores. Con el empleo cada vez más frecuente de la RNM cerebral y la angio-RNM para el estudio de estos síndromes dolorosos, la etiología vascular va cobrando cada vez más fuerza. Algunos estudios anatómicos de pacientes con neuralgia esencial del trigémino han demostrado la presencia de vasos sanguíneos comprimiendo o en contacto con la raíz en la zona de entrada en el tronco en el 91% de los casos. En un grupo control, solamente se observó en el 14% de los casos. Se postula que el contacto vascular (generalmente arterial) y su pulsación, induce pérdida de la mielina de las fibras con el resultado del aumento de la actividad aferente de esas fibras. Se propone además algún mecanismo de sensibilización central o periférico con el resultado de focos ectópicos de descarga que activan el núcleo del trigémino y sus interneuronas, resultando por ello una sensación dolorosa.
Clínicamente la neuralgia del trigémino se caracteriza por dolor agudo, eléctrico, unilateral, que afecta a una, dos o las tres ramas del trigémino. Se presenta en episodios de corta duración, múltiples a lo largo del día, alternando con períodos libres de dolor. Generalmente existe un punto gatillo en la cara, un ejemplo frecuentemente es en el surco nasogeniano. En pocas ocasiones, los pacientes definen el dolor como sordo, penetrante y continuo.
El dolor puede desaparecer espontáneamente durante meses o años. Sin embargo, los ataques son cada vez más frecuentes, más intensos y las características del dolor van cambiando, indicando probablemente que la enfermedad es progresiva, sugiriendo por lo tanto un mecanismo neuropático en su origen.
Los casos bilaterales se presentan en el 3-4% de los pacientes pero es raro que ambos lados estén activos simultáneamente.
El examen físico y neurológico generalmente es normal, aunque pueden detectarse alteraciones sensitivas en la cara y en el reflejo corneal en la neuralgia esencial. En la neuralgia secundaria o sintomática, se han observado déficits neurológicos en el 47% de los pacientes.
El diagnóstico se basa en la existencia de cuatro de los nueve criterios clínicos descritos por la Internacional Headache Society (IHS) (Tabla 3) (27).

Los estudios radiológicos complementarios, que son ineludibles, como la tomografía axial computada (TAC) y la Resonancia megnética cerebral (RMN) cerebral, van encaminados a diferenciar entre una neuralgia esencial o secundaria. La Angio-RNM es la prueba de elección para objetivar las compresiones vasculares en la zona del V par en el tronco cerebral. Algunos trabajos hablan ya de una sensibilidad cercana al 90% de los casos.
El diagnóstico diferencial se hará preferentemente con la neuralgia trigeminal sintomática en casos de tumores del ángulo ponto-cerebeloso como meningiomas, colesteatomas, tumores epidermoides, etc., con la neuralgia del glosofaríngeo, neuralgia trigeminal atípica, cefalea histamínica de Horton, neuralgia del ganglio esfenopalatino o neuropatía periférica esta última suele comenzar con parestesias y el dolores permanente, así como déficit sensitivo y/o motor en la región trigeminal y con una duración de semanas o meses. En el caso de espasmo facial se observa una contracción sincrónica paroxística aunque no dolorosa en forma de tic de todos los músculos de una mitad de la cara inervados por el nervio facial. (28)
La NT es una patología que afecta de forma importante la calidad de vida, el tratamiento farmacológico es la primera línea. Cuando la terapia farmacológica fracasa o genera efectos adversos importantes se debe considerar el intervencionismo. Se ha observado que cuanto más temprano se realice este tipo de intervenciones, mejor es el pronóstico a largo plazo. (29)
Al abordar el tratamiento de la neuralgia del trigémino lo primero que debe establecerse después del estudio de la evidencia científica de cientos de artículos publicados, es que se trata de una patología que pareciera incurable, aunque los síntomas pueden ser controlados durante años empleando tratamientos médicos y quirúrgicos. (30)
El tratamiento médico representa el primer escalón terapéutico para el control del dolor. (31)
La fenitoína fue el primer fármaco utilizado en el tratamiento de de la neuralgia del trigémino, solo hay estudios de evidencia clase III que apoyan su uso. (31, 32)
Estudios serios, clase I, han demostrado que la carbamacepina, reduce la frecuencia y la intensidad de los paroxismos dolorosos, es el fármaco más utilizado. Los efectos secundarios más frecuentes son la sedación y las alteraciones de las funciones cerebrales superiores. Un 7% de pacientes puede presentar alergia en forma de rash cutáneo. Las dosis oscilan entre 200-1200 mgr/día.(31,33,34,35,36). La oxcarbamacepina es apoyada con estudios de Clase I y meta-analisis. (31,37,38)
La lamotrigina, según estudios aleatorios, se ha demostrado efectiva, con estudios de evidencia Clase II, las reacciones cutáneas son más frecuentes. Las dosis de lamotrigina oscilan entre 200-400 mgr/día. (31,39)
El Baclofen, empleado en el tratamiento de los síndromes espásticos ha demostrado eficacia como coadyuvante a la carbamacepina en aquellos pacientes con dolor no muy intenso o con intolerancia a dosis altas de carbamacepina. La dosis diaria de baclofen oscila entre 10-80 mgr/día. La apoyan estudios de evidencia clase II. (31,40)
Otras medicaciones como el clonacepan, gabapentina, valproato sódico se han demostrado poco eficaces todavía según estudios basados en la evidencia científica clase IV. (31)
Fármacos como la tizanidina, clase II, la tocainida, clase III y el pimozide, clse III, ofrecen alguno resultados, aunque todos ellos con mayores efectos secundarios. (31,40)
El uso de lidocaína conjuntival es inefectiva. (41)
El tratamiento quirúrgico puede realizarse a tres niveles. 1.- Periférico; 2.- Ganglio; 3.- Raíz del trigémino en la fosa posterior. De todos ellos la operación a nivel de la fosa posterior es la única que no origina anestesia en alguna de las ramas del trigémino ya que es la única modalidad terapéutica quirúrgica no destructiva. Estudios que demuestran excelentes resultados en términos de alivio del dolor y duración del mismo con la descompresión microvascular en la fosa posterior. No obstante, la técnica, no es aplicable a todos los pacientes, debido en muchos casos a su edad avanzada o a la presencia de patología asociada. Existen tratamientos menos invasivos dirigidos al ganglio de Gasser tales como la rizotomía con radiofrecuencia, o la microcompresión percutánea del ganglio de Gasser con balón de Fogarty. La radiocirugía estereotáctica sobre la raíz del trigémino puede aplicarse en casos rebeldes. Otros tratamientos a nivel periférico como la crioterapia, alcoholización o neurectomías ofrecen escasas ventajas y muchas complicaciones, destacando fundamentalmente la anestesia dolorosa. La administración de glicerol en el ganglio se ha propuesto como alternativa a la radiofrecuencia pero se ha demostrado que tiene tasa elevada de fracaso y el alivio del dolor no se consigue inmediatamente (40).
La decisión de la modalidad terapéutica a aplicar debe hacerse después de analizar el estado físico del paciente, y tras la exposición de las diferentes técnicas con sus ventajas e inconvenientes, teniendo muy en cuenta la experiencia previa del médico que realizará el procedimiento quirúrgico.
Aunque existe un 29% de pacientes que solo tienen una crisis en su vida, el pronóstico de la enfermedad no es muy favorable, ya que suele ser progresiva y con el tiempo se hace más intratable, tal y como ocurre con otros dolores neuropáticos. Si se deja evolucionar, cada vez es más difícil conseguir alivio mediante los diferentes tratamientos médicos y/o quirúrgicos. (41)
A continuación ampliaremos la discusión con mayor detalle sobre las técnicas mínimamente invasivas y quirúrgicas que se utilizan actualmente para el manejo de la neuralgia del trigémino
La termocoagulación del ganglio de Gasser fue descrita por Sweet y Wepsic (10). El procedimiento posee ventajas e inconvenientes pero carece de mortalidad. El grado de recurrencia del dolor estará en función del grado de hipoestesia conseguido. Cuanto mayor es la hipoestesia generada por la lesión mayor será el riesgo de anestesia dolorosa. Las complicaciones más frecuentes son las parestesias en el 80% de los casos; debilidad del masetero (4,1%); anestesia dolorosa (1%); keratitis (0,6%), alteraciones de pares craneales III y IV, (0,8%) y mucho menos frecuente la lesión del VI par. Se muestran los resultados comparativos de diferentes series publicadas (Tabla 4) (42).

La técnica se realiza en quirófano con sedación y analgesia intravenosa, monitorización continua de la frecuencia cardiaca y la tensión arterial (bradicardia e hipertensión reactivas a la punción del ganglio de Gasser), con el paciente en decúbito supino la cabeza debe estar en hiperextensión, ligeramente girada hacia el lado contrario, con el equipo de rayos en proyección anteroposterior o ligeramente caudocraneal hasta observar el foramen oval por dentro de la línea de la articulación temporomandibular. Se marca el punto de entrada sobre la piel generalmente se encuentra a dos centímetros de la comisura labial. Se inyecta anestesia local y posteriormente se accede al ganglio con una aguja desechable de radiofrecuencia SMK C10 con 10 mm de punta activa. También es posible utilizar un kit reutilizable con cánula recta y curva de Tew. Una vez que se ha penetrado por el agujero oval, se cambia la proyección del rayo para ver la silla turca, el seno esfenoidal y el plano del clivus. Este último será el límite de profundización de la punta de la aguja. A medida que se profundiza se consiguen parestesias en las diferentes ramas siendo la primera la que está más profunda. (43)
La técnica clásica consiste en localizar la rama a lesionar mediante estimulación sensitiva a 50 Hz entre 0-1 voltio y generar posteriormente lesiones sucesivas a partir de 60º centígrados en adelante durante 60 segundos cada lesión hasta conseguir hipoestesia en la zona deseada de la cara. La lesión es dolorosa por lo que se debe sedar al paciente. (44)
Existe una nueva variante técnica conocida como radiofrecuencia pulsada, consistente en la aplicación de una corriente de radiofrecuencia pulsada, en la que no se produce lesión ya que la temperatura de los tejidos no pasa de 42º C. Los parámetros de este tipo de lesión son 2 Hz, 20 mseg., 45 voltios, 120 segundos. Generalmente se hacen dos lesiones seguidas. La información derivada de las publicaciones recientes, es que se obtienen resultados variables. Para algunos autores, el resultado de la radiofrecuencia pulsada en la neuralgia del trigémino, no es bueno debido a las altas tasas de recurrencia o no alivio del dolor, lo que obliga a repetir el procedimiento varias veces o buscar otros métodos alternativos. (45, 10)
El descubrimiento de los efectos beneficiosos del glicerol en pacientes con neuralgia del trigémino fue accidental al emplearlo como contraste en lugar de la metrizamida, para suspender los polvos de tantalio al proceder, a la radiocirugía estereotáctica (10,46). La técnica descrita originariamente ha sufrido muchas modificaciones obteniéndose mejoras en los resultados (47, 48). Según sus actuales preconizadores en el Hospital Karolinska de Estocolmo, para realizar el procedimiento el paciente debe estar sentado en una silla rotatoria. El abordaje del ganglio de Gasser se realiza por la misma vía del foramen oval descrita para la rizotomía con radiofrecuencia. La dosis necesaria es de 0,28 cc de glicerol. La selectividad de la rama a lesionar se consigue flexionando más o menos la cabeza del paciente. La Tabla 5, muestra los resultados obtenidos a largo plazo según las diferentes series publicadas empelando el glicerol.

Como se describió anteriormente, se trata de introducir un balón de Fogarty de embolectomía en el ganglio de Gasser, la técnica de entrada similar para los procedimientos de radiofrecuencia. La aguja por la que se introduce el catéter es bastante más gruesa. El procedimiento es muy doloroso por lo que es preciso anestesiar al paciente. La técnica fue descrita por Mullan y Lichtor en 1983 (12). La reacción vasovagal e hipertensiva es de esperar durante la introducción de la aguja, es un signo importante que nos revela que anatómicamente estamos en el sitio adecuado, por lo que debe estar previsto el tratamiento de la bradicardia y la hipertensión reactiva durante el procedimiento (49).
Los resultados publicados son bastante buenos (Tabla 6), Alguno autores la sugieren a pacientes que han desechado la posibilidad de la descompresión microvascular en la fosa posterior. La experiencia realizando está técnica desde hace 20 años, es que se obtienen resultados muy satisfactorios con escasa morbilidad (hipoestesia, debilidad del masetero, sin anestesia dolorosa o pérdida del reflejo corneal).
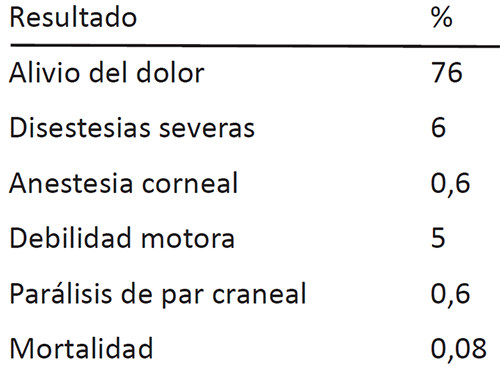
Esta técnica ha sido útil en el tratamiento de ancianos para los cuales se ha descartado la cirugía por la coexistencia de otras afecciones de salud. La compresión por balón también es la mejor elección para pacientes que tienen dolor en el nervio oftálmico o han experimentado dolor recurrente tras la descompresión microvascular. (50)
La compresión de algunos pares craneales a la salida o entrada en el tronco cerebral se ha relacionado con algunos síndromes dolorosos craneofaciales. La neuralgia del trigémino ha sido el más extensamente estudiado. Ya en el año 1932, Dandy (51), fue el primero en observar la compresión del trigémino en la fosa posterior en casos de neuralgia del trigémino. La aplicación del microscopio quirúrgico por Janetta permitió el estudio sistemático de estos problemas de compromiso neurovascular de los pares craneales describiendo una técnica para desplazar esos vasos sanguíneos sin tener que sacrificar los vasos o el nervio (7, 52)
La indicación quirúrgica según los preconizadores de la técnica es en pacientes sanos por debajo de los 65 años. En el sentir de muchos especialistas, actualmente, la decisión quirúrgica es compleja de tomar, debido a que existen procedimientos poco invasivos con resultados similares.
Los resultados quirúrgicos iniciales de las grandes series consiguen alivio completo del dolor en el 90% de los casos. Existe un riesgo de muerte en el 1% de los casos. Los resultados a largo plazo son menos favorables con porcentajes cercanos al 80%. Las complicaciones en términos de morbilidad hacen mención a infartos cerebelosos, infartos supratentoriales, infarto del allo, crisis epilépticas focales, disfunciones de pares craneales (IV, VI, VII, VIII), ataxia y alteraciones del equilibrio (53).
Mediante los equipos de aceleradores lineales que emiten rayos X o el sistema Gamma-Knife que emite rayos Gamma de una fuente de Cobalto, se consiguen también buenos resultados en casos rebeldes. Se ha publicado que esta modalidad de tratamiento (Radiocirugía) es la menos invasiva y la que presenta menos complicaciones, aunque debe confirmarse este punto en series mucho más largas (54). La radiocirugía mediante aceleradores lineales también ha demostrado su eficacia en comparación con el Gammaknife (55). Un nuevo modelo de acelerador lineal, robotizado, el CyberKnife, que no precisa marco de estereotaxia y, por lo tanto, es absolutamente no invasivo, ha empezado a emplearse en esta patología. Los resultados parecen ser bastante esperanzadores (56). La media de buenos resultados se encuentra cercana al 75% según los diferentes autores consultados. Destacan los excelentes resultados conseguidos en el alivio del dolor en la neuralgia del trigémino secundaria a esclerosis múltiple, con mejora superior al 90% de los casos (57).
Se recomienda el uso de carbamacepina u oxcarbamacepina como primera elección para el tratamiento farmacológico de la neuralgia del trigémino clásica, el baclofén y la lamotriguina quedan como segunda elección. (31)
Aunque los tratamientos quirúrgicos están soportados por trabajos de bajos niveles de evidencia, en la práctica muestran ser eficaces y aceptablemente seguros. (31)
Después de evaluar las diferentes técnicas terapéuticas para el manejo intervencionista de la neuralgia del trigémino, se debe tener en cuenta diversas variables como preferencia o condición médica del paciente, el grado de capacitación del profesional encargado de realizar la técnica elegida y el medio donde se desenvuelve, así se decidirá una técnica percutánea, quirúrgica o radioterápica. Todas ellas tienen ventajas e inconvenientes y ninguna de ellas consigue una cifra superior al 90% de éxito, en el control del dolor a largo plazo.
Los procedimientos percutáneos son más seguros, pueden ser ejecutados en pacientes con edad avanzada, pero generan adormecimiento facial, mientras que la descompresiva microvascular presenta mejor resultado a largo plazo pero involucra mayor riesgo quirúrgico y complicaciones. La radiocirugía se muestra como menos invasiva pero puede tomar semanas para ver el resultado. (31)
La técnica de microcompresión percutánea del ganglio de Gasser, motivo de este trabajo, demuestra ser un método efectivo, con resultados comparables con las estadísticas internacionales.
No requiere equipos especiales, es de bajo costo, no produce pérdida del reflejo corneal, no produce anestesia dolorosa si la compresión se realiza por debajo de cinco minutos, es útil en la neuralgia de la primera rama, es útil en la neuralgia por esclerosis múltiple, requiere corto tiempo anestésico, puede ser ambulatorio, el procedimiento es indoloro, el resultado es inmediato, con mínima morbilidad y cero mortalidad.