* Dirección: Dr. Mauricio Krivoy. Centro Médico de Caracas Edf. Anexo B, Piso 1, Cons. 1-A. San Bernardino, Caracas. Email: [email protected]
Cátedra Servicio Neurocirugía Hospital Universitario de Caracas. Hospital Privado Centro Médico de Caracas. Caracas
Se estudian los efectos de producir una lesión microquirúrgica en la zona de entrada de la raíz dorsal o DREZ-tomía en el control del dolor intratable y la espasticidad. Se definen términos, se revisa sus antecedentes históricos, sus bases anatómico-fisiológicas y se describe detalladamente la técnica quirúrgica.
Se presenta el resultado de 15 procedimientos de DREZ-tomía efectuado en 13 pacientes, 3 por espasticidad y 10 por dolor intratable. En los casos de espasticidad la etiología fue por enfermedad desmielinizante: 1 neuromielitis óptica de Devic y otro por esclerosis lateral amiotrófica. En los pacientes con dolor intratable la etiología fue diversa: 1 por schwanoma maligno ciático, 3 por aracnoiditis de la cola de caballo, 1 por miembro posflebítico, 1 por sarcoma retroperitoneal, 2 por carcinoma de cuello uterino estadios IV y IIIB respectivamente, 1 por seccion iatrogénica de S1, 1 por lesión radicular de D4 a D6 y uno por adenocarcinoma pulmonar. Los 3 procedimientos por espasticidad se obtuvo control de la misma con mejoría funcional. En los 12 por dolor intratable se logró la desaparición de este. No hubo complicaciones definitivas inherentes al procedimiento.
Se discuten los resultados y se comparan con otros procedimientos quirúrgicos, en base a ello se demuestra como DREZ-tomía es un procedimiento ablativo sobre la médula espinal de alta eficacia y baja morbilidad cuando se selecciona adecuadamente el paciente.
Efectuable con los recursos disponibles en cualquier servicio neuroquirúrgico.
Palabras clave: DREZ, dolor crónico, espasticidad.
The efects of producing microsurgical lesion in the dorsal root entry zone (DREZ-otomy) are studied, in chronic pain control and spasticity. Terms are defined. History, anatomic and physiologic basis and surgical technics are described in detail. The result of 15 Drez-otomy procedures in 13 patients is presented: 3 with spasticity and 10 with untractable pain. In the spasticity cases the etiology was demyelinating diseases: 1 Devic’s optic neuromyelitis and 1 amyotrophic lateral sclerosis. In patients with intractable pain, the etiology was diverse: 1 sciatic malignant schwanoma, 3 cauda equina arachnoiditis, 1 post-phlebitic syndrome, 1 retroperitoneal sarcoma, 2 uterine carcinoma, IIIb a IV grade respectively, 1 iatrogenic section of S1, 1 radicular D4-D6 lesion a 1 pulmonary adenocarcinoma.
In the 3 spasticity procedures the disease control was obtained with functional recovery. In the 7 cases of untractable pain relief was reached. Definitive complications were not produced. Results are discussed and compared with other surgical procedures. Based on this, it’s demostrated how DREZ-otomy is a spinal cord ablative procedure with high eficacy and low morbidity when the patient is adequately selected. DREZ-otomy can be done with available resources of any neurosurgical service.
Key words: DREZ, chronic pain, spasticity.
Aliviar el dolor ha sido uno de los anhelos y motivaciones que han impulsado el desarrollo de la medicina.
En pacientes donde el dolor se convierte en crónico e intratable, por el fracaso de la terapéutica farmacológica, la respuesta transitoria a los quimioterápicos, los efectos secundarios indeseables como en el caso de abuso de opiáceos o no encontrar respuesta satisfactoria con diversas medidas no invasivas, entre otras causas, han motivado la proliferación de diferentes técnicas quirúrgicas a todos los niveles del sistema nervioso con el objeto de interrumpir selectivamente las vías del dolor(1).
En especial, después de que en 1965 irrumpió la teoría de la Compuerta de Wall, se inició una aproximación más exacta al conocimiento del efecto de las diferentes fibras nerviosas en la modulación del impulso doloroso a la entrada del sistema nervioso central(2). Diferentes procedimientos ablativos se han desarrollado en las últimas dos décadas con sus pro y contras para cada uno de ellos(1).
En 1972 Marc Sindou, médico neurocirujano francés, introdujo el término DREZ-tomía que traduce del inglés las iniciales de Dorsal Root Entry Zone o zona de entrada de la raíz dorsal, área en la que después de múltiples estudios anatómicos se demostró la existencia de una distribución espacial específica de las fibras aferentes del dolor a la médula espinal, de acuerdo a su tamaño y mielinización(1,3).
En base a lo anteriormente expuesto, si interrumpimos microquirúrgicamente en la zona de entrada de la raíz dorsal las fibras pequeñas aferentes mielinizadas y no mielinizadas nociceptivas, la zona activadora del dolor del tracto de Lissauer junto con las primeras láminas de Rexed del asta posterior, preservando las estructuras circundantes, podemos controlar el dolor crónico sin agregar secuelas clínicamente significativas al paciente(3).
Como consecuencia de los primeros casos realizados del procedimiento en cuestión, se observó una disminución significativa de los reflejos miotáticos en los territorios operados, por lo que en 1973 Sindou utilizó la misma técnica como tratamiento de pacientes con problemas de espasticidad severa en miembros superiores con resultados satisfactorios(3,4), lo que motiva a que se incluye en este estudio la aplicación de la técnica DREZ-tomía en pacientes con espasticidad.
El objetivo de este trabajo de investigación es difundir la DREZ-tomía como técnica quirúrgica aplicable con los recursos disponibles en el hospital, de baja morbilidad y alta efectividad cuando se seleccionan adecuadamente los pacientes. Dar pautas prácticas en cuanto a la selección del paciente y obtener conclusiones con respecto a la utilización de la técnica.
Se denomina desde el punto de vista anatómico como zona de entrada de la raíz dorsal (DREZ) al segmento radículo-medular compuesto por la porción central de la raíz dorsal, las primeras 5 láminas de Rexed del asta posterior donde está incluida la sustancia gelatinosa de Rolando (SGR) y el tracto de Lissauer (TL). En esta área anatómica es donde las fibras aferentes hacen sinapsis con los grupos neuronales que originan la vías ascendentes extralemniscales(1).
Existen terminaciones nerviosas libres profusamente ramificadas cubiertas de células de Schwan por debajo de la epidermis sindicadas de ser las responsables de la captación del estímulo doloroso. Asimismo cualquier estímulo suficientemente intenso es capaz de evocar dolor. La aferencia dolorosa alcanza los centros medulares a través de la neurona sensitiva cuyo soma se encuentra en el ganglio de la raíz dorsal mediante dos tipos de fibras. Unas muy finas, no mielinizadas, llamadas fibras C de 0,4 a 1,1 micras de diámetro. Otras, las fibras delgadas mielinizadas A-delta, de 1,0 a 5,0 micras de diámetro(15).
La raíz dorsal se divide en: 4 a 10 raicillas de 0,25 a 1,5 mm de diámetro cada una, compuestas de dos partes embriológicamente distintas, una de sistema nervioso periférico y otra central, separadas por el anillo pial de Tarlov a 1 mm de distancia antes de penetrar al surco dorso-lateral medular. Cada raicilla posee la misma proporción de fibras en diámetro y mielinización que la raíz original, por lo que se le pueden considerar como una unidad anatómico funcional(16).
En el segmento periférico las raicillas no tienen ninguna distribución específica de sus fibras, a diferencia del segmento central donde la mayoría de las fibras de pequeño diámetro, consideradas nociceptivas, se reagrupan lateralmente antes de penetrar en el tracto de Lissauer. De lateral a medial siguen en orden las fibras que van al asta posterior a formar las vías lemniscales, luego las fibras que penetran la sustancia gris hacia el asta anterior y son responsables de los reflejos miotáticos junto con fibras propioceptivas(1) (Figura 1).
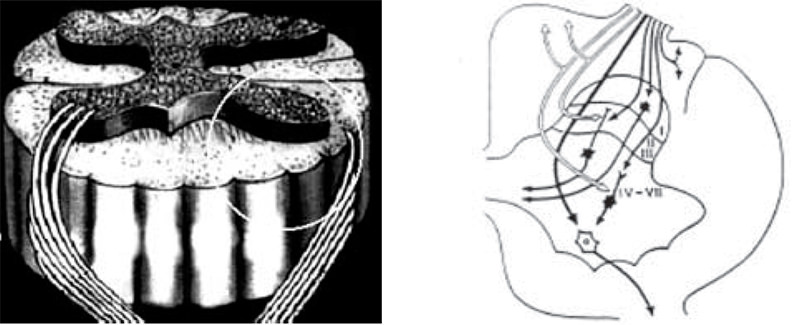
En el asta posterior, después de atravesar el tracto de Lissauer, las fibras A-delta llegan a la lámina I de Rexed o capa celular marginal de Waldeyer. Las fibras C terminan en la lámina II de Rexed o sustancia gelatinosa de Rolando. Un pequeño grupo de fibras terminan en la lámina V. La neurona secundaria se interconecta con el asta anterior o lateral del mismo nivel para los reflejos somáticos o autonómicos respectivamente. Otras neuronas secundarias, conductoras de dolor, se proyectan contralateralmente hacia niveles superiores. Es de hacer notar que los axones de cada dermatomo se decusan de uno a tres niveles por encima del nivel de entrada de la raíz por lo que el asta posterior y la comisura espinal anterior se comportan como verdaderas vías de paso al dolor. Estas fibras cruzadas se van agregando al tracto espinotalámico contralateral en su porción interna a medida que ascendemos en la médula, siendo las fibras sacras las más externas del haz espino-talámico y las cervicales las más internas. Dichas fibras se proyectan vía lemnisco medio al núcleo ventropostero-lateral del tálamo principalmente y en menor número de ellas a los núcleos ventro-postero-medial, interlaminares y ventro-basales para luego dar sus eferencias hacia la corteza cerebral(15).
El tracto de Lissauer, situado dorso lateral al asta posterior está compuesto por dos partes. Un segmento medial donde las fibras pequeñas que llegan, se trifurcan para alcanzar el asta posterior hasta dos metámeras por encima o debajo del nivel de la entrada de la respectiva raíz. El otro segmento, lateral, compuesto por fibras propio-espinales que interconectan distintos niveles de sustancia gelatinosa entre sí. Esto demuestra el papel importante que tiene el tracto de Lissauer en la modulación intersegmentaria del dolor. Trasmite el efecto excitatorio de las fibras nociceptivas a través del segmento medial y lleva la influencia inhibitoria de la sustancia gelatinosa de Rolando entre metámeras vecinas(1)
En 1965, Melzack y Wall dieron a conocer un modelo teórico que explica la modulación del estímulo nociceptivo en la entrada al sistema nervioso central conocido como la teoría de la compuerta. Ellos observaron que la estimulación periférica de las fibras mielinizadas producían potenciales negativos en la zona de entrada de la raíz dorsal, mientras que la estimulación de las fibras C originaban potenciales positivos. Estas observaciones los llevó a establecer la existencia de interneuronas que actúan de forma inhibitoria sobre las células de transmisión del dolor. Estas interneuronas a su vez serían influenciadas en forma negativa por las fibras C, y estarían estimuladas por las fibras mielinizadas y por centros cefálicos. Posteriormente Wall en 1980 afinó su teoría, situó las neuronas de transmisión en la lámina V del asta posterior y las interneuronas inhibitorias en las láminas II (sustancia gelatinosa) y III de Rexed. La esencia de la teoría consiste en que las fibras mielinizadas producen activación de las células inhibitorias capaces de producir inhibición presináptica de las células de transmisión, contrariamente las fibras C, inhiben las interneuronas inhibitorias, dejando las células de transmisión en estado excitatorio (Figura 2)(1,15,17).
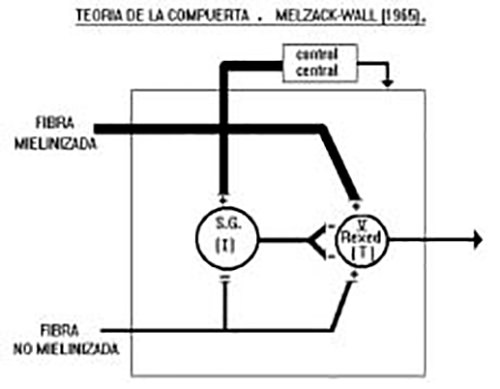
Todo el anterior sistema de conexiones descrito trabaja mediante mediadores químicos encargados de la neurotrasmisión del dolor bajo el término de “sistema endógeno de analgesia”, introducido por Reynolds en 1969, quien encontró que estimulando eléctricamente la sustancia gris pe-riacueductal producía una profunda analgesia que en estudios posteriores se demostró un efecto inhibitorio sobre las láminas I y V de Rexed en el asta posterior, efecto similar al producido por los opiáceos. Un grupo de péptidos naturales han sido aislados en el sistema nervioso central semejantes a morfina llamados endorfinas, entre las que se encuentran las betaendorfinas, las beta lipotropinas y las encefalinas. A nivel del asta posterior se encuentran receptores para encefalinas involucrados en los fenómenos inhibitorios del dolor, mientras un 11-amino-péptido denominado sustancia P, incrementa su concentración a la llegada del impulso nervioso al asta dorsal(15,17).
De lo anterior se deduce que cuando existe una lesión que altere las aferencias ya sea a nivel del nervio periférico, raíz dorsal o parénquima medular que disminuya el efecto inhibitorio de las fibras mielinizadas sobre el asta posterior o altere el equilibrio del sistema endógeno de analgesia, entonces prevalecerá un efecto excitatorio sobre las neuronas de transmisión, las que por estudios electrofisiológicos se encuentran en continua descarga, con patrones de actividad neuronal epileptiforme, siendo este el sustrato fisiopatológico del dolor de deaferentación(1,15,18-20).
Basado en los fundamentos teóricos antes descritos y sus estudios anatómicos originales, específicamente la distribución espacial de las aferencias nociceptivas a la médula, en 1972 el Dr. Marc Sindou, en Lyon, Francia, introdujo el concepto de cirugía en la zona de entrada de la raíz dorsal. Postula que si se produce una lesión microquirúrgica en esta zona, sobre el surco dorso lateral medular en su porción ventral, buscando lesionar las aferencias nociceptivas traídas por las fibras pequeñas mielinizadas y no mielinizadas que corren laterales en el segmento central de la raíz dorsal junto con la porción medial excitatoria del tracto de Lissauer y las primeras láminas del asta posterior, preservando parcialmente las estructuras inhibitorias del asta posterior y las fibras propio-espinales del tracto de Lissauer lateral que interconecta la sustancia gelatinosa a distintos niveles metaméricos, entonces podemos producir analgesia con preservación al menos parcial de la sensibilidad tactil y la propioceptiva para evitar fenómenos de deaferentación con conservación las vías motoras en casos de dolor intratable(1,3,4).
Como consecuencia de los primeros casos de DREZ-tomía efectuados, se observó una disminución marcada de los reflejos miotáticos en los territorios operados, por lo que en 1973 Sindou utilizó la misma técnica como tratamiento de pacientes con espasticidad en miembros con adecuados resultados(3,4).
El sistema músculo-esquelético mantiene una retro-alimentación continua de información con el sistema nervioso central. Existen dos tipos de receptores periféricos, uno el órgano tendinoso de Golgi y el otro los receptores espirales musculares. El órgano tendinoso de Golgi se encuentra en la unión músculo-tendón conectado en serie. Este órgano es capaz de captar la tensión generada por el músculo, dando una respuesta dinámica. Su aferencia va por fibras mielinizadas grandes tipo Ib y produce respuesta inhibitoria sobre el músculo estimulado y excitatoria del antagonista. Los receptores espirales musculares se encuentran en paralelo con las fibras del músculo, responden a la longitud de estiramiento dando una respuesta estática. Mantienen dos tipos de aferencias una va por las fibras produciendo una respuesta excitatoria al músculo agonista, monosináptica e inhibitoria al antagonista, disináptica. La otra aferencia se conduce por fibras tipo II que siempre excita los flexores, siempre inhibe los extensores y a veces tiene cierta capacidad de excitar algunos grupos de extensores. Estos receptores musculares reciben una eferencia a través de las fibras gamma que contraen las fibras intrafusales aumentando la sensibilidad de respuesta del sistema. La motoneurona superior regula de forma inhibitoria el sistema de control de los reflejos miotáticos(21).
Desde el punto de vista neurofisiológico la espasticidad es una respuesta exagerada de los reflejos miotáticos que se traduce desde le punto de vista clínico en reflejos hiperactivos, aumento de la resistencia muscular en proporción lineal a la velocidad de estiramiento pasivo del músculo, afectación predominante de los músculos antigravitatorios. Flexión-pronación de los miembros superiores y extensión-adducción de los miembros inferiores. El músculo puede mantenerse normotónico en reposo pero inmediatamente al producirse un estiramiento este responde con una contractura en aumento proporcional a la tracción hasta un punto donde la resistencia cede abruptamente conocido como signo de la navaja. El clonus acompaña la signología(21,22).
Cuando existe una lesión que altere las vías descendentes de la motoneurona superior no sólo se produce la pérdida del estímulo inhibitorio de ésta sobre la motoneurona inferior alfa por un fenómeno liberación, sino que recientemente se ha evidenciado que existe una actividad facilitadora de los receptores espirales incrementando la actividad tónica sobre las motoneuronas gamma. También se ha descrito potenciales tónicos espontáneos de las motoneuronas alfa regulados por los sistemas retículo y vestíbulo espinal(22).
Conociendo el efecto excitatorio de las aferencias miotáticas en el fenómeno espástico y la segregación espacial de las fibras en la zona de entrada de la raíz dorsal es fácil de entender el fenómeno observado por Sindou. Las fibras mielinizadas grandes miotáticas corren mediales a las nociceptivas a la entrada al sistema nervioso central. Cuando se realiza la DREZ-tomía quedan incluidas en el área de la lesión las fibras miotáticas, eliminando el arco aferente de los reflejos de estiramiento siendo esta la base anatómico-funcional de la técnica quirúrgica estudiada en el tratamiento de la espasticidad(3,4,23) (Figura 3).

Los pacientes seleccionados fueron operados bajo anestesia general haciendo siempre la salvedad al anestesiólogo de utilizar relajantes musculares de corta duración de manera de garantizar que el paciente no esté relajado en el momento de la estimulación de la raíz motora para la determinación del nivel metamérico a intervenir. El paciente se posiciona en decúbito ventral sobre apoyos torácicos e ilíacos sea con almohadas o sobre el arco de Wilson. La cabecera de la cama quirúrgica descendida unos 20 grados para evitar excesiva pérdida de líquido cefalorraquídeo. La posición sentada puede ser utilizada en casos de abordaje de la columna cervical. El nivel vertebral se localiza por palpación de las apófisis espinosas y en caso de dudas se marca el nivel utilizando los rayos X. Se procede a realizar la laminectomía total bilateral con la técnica habitual, en lo posible con preservación de las apófisis espinosas. Se laminectomiza de T10 a L2 en casos de necesitar exponer el cono medular en patología dolorosa lumbo-sacra. La duramadre y la aracnoides se abren de forma longitudinal, refiriéndose lateralmente con seda 4-0 para mantener el campo quirúrgico amplio.
La identificación del nivel radicular se realiza desde cervical hasta L2 siguiendo la raíz hacia su salida por su respectivo agujero de conjunción. A nivel lumbo-sacro se utilizó el estimulador de nervio Vari-Stim® III de la Concept con tres niveles de intensidad: 1/2, 1 y 2 mA para la estimulación motora, con el paciente sin efecto de relajantes musculares. En los dos últimos procedimientos se realizó la estimulación radicular con la pinza de bipolar.
Siempre iniciando con la mínima intensidad.
Las raíces dorsales cervicales están una a continuación de la otra, pero su salida por el agujero de conjunción está al mismo nivel. A diferencia de las torácicas donde encontramos un espacio libre entre un nivel radicular y otro, pero su salida por el agujero de conjunción es generalmente dos niveles vertebrales por debajo. Estos espacios libres también se deben incluir en casos de DREZ-tomía dorsal(24).
A nivel lumbo-sacro, la identificación del nivel no resulta sencilla debido a la forma de emerger agrupadamente las raíces en el cono medular, ininterrumpidamente una al lado de la siguiente. La salida de la raíz, en especial de L3 hacia abajo es muy caudal a su emergencia del cono medular, lo que impide su seguimiento hacia su respectivo agujero de conjunción para utilizarlo como referencia anatómica.
Algunos detalles técnicos son de importancia para la orientación anatómica a nivel lumbo-sacro. L1 y L2 pueden ser seguidas hasta sus respectivos agujeros de conjunción. La estimulación eléctrica de L2 produce respuesta del grupo ilio-psoas y adductores. La estimulación eléctrica de S1 produce contracción del grupo muscular gastrocnemio-soleo inclusive si se estimula la raíz dorsal. En S2, S3 y S4 se produce respuesta anal y vesical(3).
La raíz S1 en su porción dorsal es más gruesa que el resto de las raíces sacras que le continúan(24). Otra referencia anatómica de importancia, basada en estudios post-mortem ha demostrado que el nivel S1-S2 se encuentra a 30 mm por encima de la salida de la muy fina raíz coccígea. Nivel de suma importancia para la preservación de la función vesical(3).
Una vez localizado el nivel indicado, se introduce el microscopio quirúrgico y las raíces dorsales son rechazadas dorso-medialmente para obtener buena visualización del surco dorso-lateral. Para ello las adherencias aracnoideas deben ser cuidadosamente disecadas. Una vez expuesto el surco dorso-lateral, los pequeños vasos piales son coagulados con bipolar. La arteria espinal postero-lateral corre sobre el surco dorso-lateral, su diámetro oscila entre 0,1 y 0,5 mm. Es alimentada por ramos dorsales de las arterias radiculares y se anastomosa caudalmente con la arteria de Adamkiewicz a través del sistema anastomótico del cono medular de Lazorthes. Estos vasos deben ser delicadamente disecados y preservados cuando están presentes. Una vez coagulados los vasos piales, se procede a abrir la membrana pial con tijera de microcirugía curva. Luego, utilizando un bisturí con hojilla 11, al que previamente se le marcó una distancia desde su punta de 2 mm, se realiza la surcotomía con la profundidad preestablecida de 2 mm y un ángulo de 45 grados en sentido ventro-medial. Con la pinza de bipolar de microcirugía, los bordes de la lesión son suavemente separados hasta encontrarnos con la sustancia gris del asta posterior. La DREZ-tomía se completa con pequeñas microcoagulaciones de la incisión realizada(1,3,4).
La duramadre se cierra de forma hermética, seguida de una maniobra de Valsalva para descartar la fuga de líquido cefalorraquídeo. Se reponen las apófisis espinosas en caso de haberlas preservado. La aponeurosis, el subcutáneo y la piel se suturan con la técnica habitual.
Se utilizó esteroides y antibióticoterapia peroperatoria(24).
En el estudio realizado finalmente se seleccionaron 13 pacientes, 10 femeninos y 3 masculino, cuyas edades se encuentran entre 17 y 61 años (media de 39,5 años), quienes fueron sometidos a la técnica quirúrgica de DREZ-tomía, 11 unilateral y 2 bilaterales (casos 2 y 5), totalizando 15 procedimientos ejecutados.
Se practicaron 3 procedimientos en 2 pacientes por espasticidad ambos secuelares, uno a neuromielitis óptica de Devic y otro a esclerosis lateral amiotrófica, este último con espasticidad dolorosa (bilateral), y 12 procedimientos en 11 pacientes con dolor intratable por las siguientes causas: 3 por aracnoiditis de la cola de caballo, schwanoma maligno del nervio ciático, miembro posflebítico (bilateral), sarcoma retroperitoneal indiferenciado, 2 casos por carcinoma de cuello uterino uno estadio IV y otro estadio III B, sección iatrogénica de S1, lesión radicular de D4-D6 y un caso de adenocarcinoma pulmonar. El tiempo de evolución de la enfermedad de base varió entre 3 meses y 30 años.
Entre los intentos previos de terapéutica se encuentra el uso de fisioterapia y baclofén en los casos de espasticidad, de analgésicos antiinflamatorios no esteroideos en todos, laminotomía con debridación de aracnoiditis, infiltraciones, catéter peridural, 2 simpatectomías y el uso de opiáceos como morfina, propoxifeno (Algafan®) o Nalbufina (Nubain®).
Se realizaron: 2 laminectomía cervical, 1 dorsal, 2 lumbar y 8 dorso-lumbares. En 6 pacientes se preservaron las apófisis espinosas. Se utilizó el estimulador de nervios para la orientación del nivel radicular en 12 procedimientos, en 2 se realizó con el bipolar a la mínima intensidad (procedimiento 9 y 10).
Como hallazgos intraoperatorios se encontró ausencia del surco dorso-lateral (caso 5). La presencia de un ramo arterial, arteria anastomótica de Lazorthes, ocupando dicho surco en el lado izquierdo (caso 6) y lado derecho (caso 8). Ausencia del plexo venoso sobre el surco dorso-lateral (caso 6).
De los 15 procedimientos de DREZ-tomía ejecutados, el nivel radicular operado fue a nivel cervical en dos casos, de C4 a C6 y C7-C8, uno dorsal de D4 a D6 cuatro a nivel lumbar puro de L3 a L5 bilateral y L2 a L5 y ocho procedimientos lumbosacros L4 a S1 bilateral, L1 a S1, L3 a S3 y L4 a S3.
De los pacientes con espasticidad en ambos desapareció la misma, en el caso 1 con recuperación funcional del miembro superior izquierdo que le permiten actividades como comer, peinado o cepillado dental. En el caso # 2 además sin dolor, prevaleció el déficit motor existente pero facilitando las maniobras de cuidado diario.
En los pacientes con dolor, en todos hubo desaparición del mismo desde el posoperatorio inmediato, exceptuando el caso 5, con DREZ-tomía bilateral, asintomático del lado izquierdo, refirió dolor en los 3 dedos medios del pie derecho el que desapareció a las 48 horas de posoperatorio. Único paciente que recibió una dosis de opiáceo en el posoperatorio y que coincide con la variante anatómica de ausencia del surco dorso-lateral derecho.
Al examen físico posoperatorio de las metámeras sometidas a cirugía se encontró analgesia a estímulos dolorosos, hipoestesia de leve a moderada y disminución de la propiocepción la que desaparece progresivamente. En los pacientes que existía lesión previa con anestesia dolorosa queda área de anestesia.
Se evidenciaron como complicaciones transitorias inherentes al procedimiento paresia en el caso #3 con resolución a las 3 semanas, caso 5 lado derecho que coincide con la variante anatómica de ausencia del surco dorso lateral y caso 7 con restitución a la semana que coincidió con la utilización durante el acto operatorio de una pinza de bipolar de mayor diámetro a la usual. En el caso 8 se presentó salida de líquido cefalorraquídeo por la herida operatoria desde el día 3 al 8 del posoperatorio acompañado de cefalea y nucalgia las primeras 24 horas por hipotensión del líquido, se resolvió con drenaje por punción paralela a la herida y cura compresiva, paciente con posible compromiso de la cicatrización por haber recibido radioterapia externa, implantes radioactivos y dos ciclos de quimioterapia.
No se observaron alteraciones del trofismo sino por el contrario al eliminar el dolor y facilitarse la movilización o deambulación del paciente se observó disminución de las úlceras maleolares de 18 años de evolución en el caso 5, paso de las úlceras por apoyo de húmedas a costrosas en el caso 6 y resolución del gran edema de todo el miembro inferior derecho en 2 días en el caso 7.
De 15 procedimientos se logró el seguimiento inicial de 13 de ellos (caso 6 sin seguimiento). El tiempo varió entre 3 y 27 meses con una media de 13 meses. Sin recidiva de ninguno en este primer período.
En 5 de los pacientes se ha logrado un seguimiento de hasta 6 años, dos de ellos con procedimiento bilateral, total 7 procedimientos. El caso 5, con dolor por miembro posflebítico, operado bilateralmente se mantiene asintomático del lado izquierdo y refiere dolor a nivel S1,S2 derecho. El resto de los pacientes seguidos se encuentran sin recidiva.
No hubo complicaciones definitivas ni mortalidad inherente al procedimiento quirúrgico.
En el paciente con dolor y/o espasticidad, la decisión de llegar a un tratamiento quirúrgico no resulta sencilla. Se debe conocer bien al paciente y su enfermedad de base, realizar una evaluación neurológica y neuropsicológica meticulosa(25), revisar los procedimientos terapéuticos a los que ha sido sometido y valorar el grado de incapacidad o déficit que la patología origina. Sólo entonces es cuando podemos pensar en someterlo a un plan de tratamiento quirúrgico seleccionando las opciones de menor riesgo de morbi-mortalidad y mayor eficacia.
La Asociación Americana de Neurocirujanos en su sección de dolor, en el congreso anual de 1993, organizó un grupo de conferencias para llegar a un consenso sobre el manejo neuroquirúrgico del dolor. Se clasificaron los procedimientos en tres categorías:El neurocirujano es el único especialista calificado para proveer estas opciones de tratamiento definitivo en casos de dolor crónico, persistente e intratable, aunque el manejo del mismo sea de un equipo médico multidisciplinario(26).
Los resultados obtenidos en el presente estudio se muestran como una contribución que corrobora la eficacia de la DREZ-tomía, como procedimiento ablativo sobre la médula espinal, en el control del dolor y/o espasticidad que han fracasado a diversos intentos terapéuticos.
En todos los pacientes sometidos al tratamiento quirúrgico se obtuvo un excelente resultado tanto en los 3 procedimientos por espasticidad como en los 12 por dolor intratable. Si bien el número de casos puede no ser suficientemente extenso para generalizar conclusiones, los resultados finales son muy llamativos, los que definitivamente se lograron por la cuidadosa selección de los pacientes a ser intervenidos. Una historia clínica detallada con un examen físico cuidadoso, el conocimiento de la enfermedad de base en la etiopatogenia del dolor y la corroboración con los estudios paraclínicos fueron la clave de la adecuada escogencia de los pacientes.
El dolor neurogénico puede manifestarse en tres presentaciones(2):
En series estudiadas por Sindou, especialmente en pacientes con cáncer, el resultado es superior cuando se trata pacientes con alodinia o dolor espontáneo (88 % de buenos resultados) con respecto aquellos con dolor permanente(2). Esta observación se evidenció en los resultados donde la sensación de mejora del paciente es más dramática en los que presentaron alodinia como dolor predominante.
Al examinar los pacientes sometidos a DREZtomía se observó analgesia como el cambio más relevante en la sensibilidad, además de hipoestesia de leve a moderada y disminución de la propiocepción que mejora en pocos días, cambios todos limitados a las metámeras intervenidas. Estos datos aportan evidencia suficiente de la selectividad de la técnica en el control del dolor en comparación con otros procedimientos como las cordotomías o rizotomías(2).
Ninguna de las complicaciones inherentes al procedimiento quirúrgico fue permanente, de los 3 procedimientos que cursaron con paresia transitoria, uno presentaba la variante anatómica de no existir surco dorso lateral como tal (caso 5, procedimiento 7) por lo que la lesión medular se realizó sobre el área teórica de su ubicación y el otro (caso 7, procedimiento 9) se utilizó una pinza de bipolar para producir la lesión más ancha de lo usual, por problemas técnicos del instrumental, lo que podría explicar por lesión de mayor dimensión, la aparición de paraparesia. El déficit de mayor duración fue de 3 semanas con recuperación total. La otra complicación obtenida (caso 8, procedimiento 10), fue la salida de líquido cefalorraquídeo por la herida operatoria, de bajo volumen, desde el día 3 al 8 del posoperatorio, en una paciente que previamente recibió radioterapia externa, implantes radioactivos y dos ciclos de quimioterapia, procedimientos que comprometen el proceso de cicatrización normal. Se controló con punción paralela a la herida operatoria y cura compresiva.
Diversas anomalías están descritas en esta área anatómica y sus proximidades. En series como la de Kadish y Simmons alcanzan el 14 % de la autopsias revisadas(27), algunas con relativa alta frecuencia como la duplicación de raíz(28,29).
Para corroborar el nivel metamérico sobre el cual estamos realizando el procedimiento ablativo, el grado de destrucción que practicamos y la funcionalidad del tejido nervioso circundante, en especial en casos de encontrarnos con variantes anatómicas, es recomendable en lo posible la monitorización durante el acto quirúrgico con potenciales evocados incluso epidurales(30), o mediante el uso de estimulación y electromiograma, ya sea en los casos de tratamiento por dolor o por espasticidad(31,32).
Diversas formas de producir lesión quirúrgica sobre el sistema nervioso están descritas. Específicamente en DREZ-tomías, a parte de la técnica mencionada en este trabajo que se corresponde a la original diseñada por el Dr. Marc Sindou, utilizando técnicas de microcirugía con bisturí y bipolar(1-4), las lesiones sobre la zona de entrada de la raíz dorsal pueden ser practicadas con radiofrecuencia, técnica difundida por el Dr. Blaine Nashold, quien sugiere el uso de electrodos de 0,25 mm de diámetro, a 2 mm de profundidad, entrando en el surco dorso-lateral en su parte medial con 25 grados de angulación, a una temperatura de 70 grados centígrados por 15 segundos, se producen lesiones a intervalos de 2 a 3 mm, con estos parámetros logra áreas de coagulación de 4 a 5 mm de diámetro(9-11,24,33).
El otro método utilizado para producir lesión en la zona de entrada de la raíz dorsal es el láser de dióxido de carbono, descrito inicialmente por el Dr. Walter Levy, con parámetros de 20 watts, fijando el diámetro del rayo de aproximadamente 0,4 mm y 0,1 segundo de duración a un ángulo de 25 grados(12-14,34).
Existen controversias sobre las ventajas y desventajas del uso de un método sobre los otros. La técnica original tiene la ventaja de poder ser practicada con el instrumental usual de microcirugía y la magnitud de la lesión producida es controlada bajo visión directa. Con el uso del láser y de la radiofrecuencia el primer inconveniente es la disponibilidad de los costosos equipos. A la radiofrecuencia se le asigna la desventaja de menor reproductibilidad de las características de las lesiones y de producir mayor edema peri-lesional(35). El láser si bien tiene mayor precisión, el efecto de la onda de pulso y de respiración sobre la médula, produce desplazamiento de esta que pudiera modificar el blanco del rayo(14). Existen dificultades de técnica quirúrgica durante el uso de láser de dióxido de carbono como lo es lograr un campo quirúrgico seco, sin líquido cefalorraquídeo, disección cuidadosa de los vasos y la posibilidad de una adecuada angulación del equipo en la incidencia del rayo(36). A nivel experimental en gatos se ha descrito alta frecuencia de aparición de siringomielia con el uso del láser sobre la zona de entrada de la raíz dorsal(37).
Haciendo la comparación de la DREZ-tomía con los diversos tipos de procedimientos neuroquirúrgicos en cuanto a indicaciones y resultados, encontramos que con respecto a los procedimientos neuroaumentativos, la estimulación eléctrica espinal está indicada en radiculopatía por síndrome poslaminectomía, neuropatía periférica, enfermedad vascular periférica y síndrome posamputación. Con un resultado a largo plazo de 50 % a 60 % de éxito(26). Tiene las ventajas de ser reversible, controla el dolor bilateralmente y permite realizar una prueba per o trans-cutánea para valorar previo implante definitivo la efectividad del mismo(26,38-44). Presenta las desventajas de ser un cuerpo extraño implantado, de producir en ocasiones sensación vibratoria displacentera y de disminuir la efectividad con el paso del tiempo, descrito tanto por fibrosis que suele envolver el electrodo aislándolo, como por plasticidad del sistema nervioso que crea tolerancia(45).
El otro grupo de procedimientos neuroaumentativos consiste en la administración de drogas intratecales tanto por vía percutánea si la esperanza de vida es menor de tres meses o por implante de bombas y reservorios subcutáneos si la expectativa es mayor. En caso de dolor, está descrito el uso de anestésicos, clonidina, esteroides entre otros(46), pero sólo el sulfato de morfina libre de preservativos es el único aprobado para uso intratecal por la Administración de Drogas y Alimentos de Estados Unidos de América (FDA)(26). Tienen la misma ventaja que la neuroestimulación, con las desventajas presentar aumentos progresivos de los requerimientos, posibilidad de intoxicación por sobredosificación, se presentan síndromes por retiro del medicamento y el paciente debe volver periódicamente al centro hospitalario para el recargo de la bomba de infusión(26,47). En Venezuela no hay disponibilidad de morfina libre de preservativos para uso intratecal.
En casos de espasticidad el baclofén intratecal es una opción que surgió a consecuencia del fracaso de la terapéutica vía oral y de ciertos procedimientos ablativos, se describe gran variabilidad de respuesta de paciente a paciente, con poca aparición de tolerancia. Se recomienda en casos de espasticidad de extensos territorios con fracaso al tratamiento vía oral. También se menciona el uso de morfina y midazolan con resultados alagadores pero de corta duración(8,48,49).
Entre los procedimientos ablativos sobre la médula espinal diferentes a la DREZ-tomía, tenemos la cordotomía antero-lateral, ha presentado resultados positivos en casos de enfermedad maligna con dolor lancinante, paroxístico más que dolor continuo. En casos de enfermedad no maligna tiene pocas indicaciones. Presenta amplias complicaciones que incluye lesión del tracto córtico-espinal con espasticidad y/o paraparesia hasta en el 15 % de casos unilateral y 39 % en bilateral. No es selectivo a un nivel metamérico específico. Incontinencia urinaria en el 5 % de los casos unilateral y 25 % de los casos bilaterales. Depresión respiratoria más en cordotomía cervicales así como apnea del sueño. Hipotensión ortostática hasta del 36,1 %. Cursa con cifras hasta del 6 % de mortalidad, mayor si es cervical y bilateral. Se describe dolor contralateral en espejo tipo disestesia en el 16 %. Síndrome de Horner que desaparece con el tiempo. Presenta recidivas significativas, por lo que se recomienda en casos de enfermedad maligna con corta expectativa de vida. Buenos resultado a largo plazo de hasta 66 %. El abordaje percutáneo y con radiofrecuencia está descrito, con reducción de la mortalidad al 3 %(1,26,50,51).
La mielotomía comisural media es reportada como efectiva en el tratamiento de dolor sacro o pelviano debido a malignidad por su alta recurrencia. La ventaja que presenta es que con una sola lesión puede controlarse el dolor bilateralmente, como complicaciones, la disfunción de las columnas posteriores, paresia hasta en el 44 %, incontinencia urinaria del 11 % al 35 % y sensación displacentera hacia el dermatomo más distal intervenido, disestesias o hiperalgesia que tiende a disminuir, son las más frecuentes(1,26,52). Se ha reportado el uso del láser y el ultrasonido para realizarla(1,53).
La mielotomía longitudinal establecida para casos de espasticidad, es menos específica que la DREZtomía por producir lesión bilateral, tiene mayor incidencia de disfunción urinaria, se recomienda en casos de lesión medular completa con espasticidad severa que dificulta el cuidado del paciente(5-7).
La rizotomía es un procedimiento ablativo fuera de la médula espinal, pero su uso está extendido tanto en casos de dolor: rizotomía posterior o en casos de espasticidad: rizotomía anterior y/o posterior. Presenta las ventajas de ser un procedimiento técnicamente sencillo de baja morbi-mortalidad y limitado al dermatomo específico requerido. Tiene las desventajas de producir lesión total de la sensibilidad en casos de la rizotomía posterior o lesión total de la motilidad en la rizotomía anterior. Aumenta el riesgo de trastornos tróficos y los buenos resultados iniciales se ven disminuidos con el tiempo por la posibilidad de aparición de dolor secundario a la deaferentación(4,54-58). Las rizotomías parciales, el uso de la radiofrecuencia y el abordaje percutáneo han agregado mejoras a la técnica y resultados(59-61).
Realizar una comparación con los anteriores procedimientos ablativos descritos sobre la médula espinal y raíces resulta difícil debido a la gran variedad de patologías que están involucradas y a la diversidad de autores con criterios personales que las exponen. La DREZ-tomía con la técnica original con bisturí y bipolar bajo microscopio presenta las ventajas de ser un procedimiento técnicamente sencillo, que no amerita disponibilidad de grandes recursos, es selectivo a las metámeras afectadas y respeta el lado contralateral. Daño piramidal definitivo está reportado hasta el 1 %, no se observó en la casuística presentada. No debe producir trastornos esfinterianos si se respetan los límites anatómicos sacros. Tiene una mínima mortalidad, menor al 1 %, inherente al procedimiento quirúrgico. Presenta baja recidiva a largo plazo y alta eficacia en comparación a otros métodos, con buenos resultados de hasta el 88,2 % en casos de dolor y 78,9 % en espasticidad. No altera el trofismo de las metámeras operadas y es selectivo a la sensibilidad dolorosa aunque se acompañe en ocasiones de hipoestesia y cambios en la propiocepción que mejoran con el tiempo(1-4,9,10,16,17,24,61).
El procedimiento quirúrgico de DREZ-tomía no sólo se limita a dolor o espasticidad en miembros, sino también tiene indicaciones en el tratamiento del dolor facial realizándose a nivel del núcleo caudalis en la unión bulbo-medular, reportado por primera vez por Nashold en 1985, con radiofrecuencia, presentando 90 % de buenos resultados inmediatos y 58 % a largo plazo(24,26,63,64). Asimismo en casos de vejiga neurogénica espástica la DREZ-tomía se presenta como alternativa terapéutica. Se practica en las metámeras sacras de S-2 hacia caudal con resultados positivos de hasta el 75 % de mejoría en la capacidad de almacenamiento urinario(2).
Los grandes avances en neurociencias, el entendimiento de las bases anatómicas y fisiológicas del dolor y de la espasticidad, un número importante de procedimientos se han desarrollado para el manejo cuando estos se vuelven crónicos o intratables. Sin embargo, la mayoría de dichos procedimientos no han sido sometidos a ensayos clínicos rigurosa y científicamente controlados debido a múltiples factores. Entre ellos tenemos que un procedimiento quirúrgico es algo muy variable y no puede ser sometido a controles tipo doble-ciego o practicar procedimientos placebos como si lo es posible con ensayos farmacológicos. Además, el síndrome doloroso es muy variable, está influenciado por factores no fisiológicos locales como los psicológicos o sociales y lo más importante, el dolor es una experiencia individual y subjetiva(25). Por lo anteriormente expuesto, persiste incertidumbre en el ámbito médico y más aún neuroquirúrgico, del papel que juegan los procedimientos ablativos sobre la médula espinal en el control del dolor y/o espasticidad(26) contribución que aporta el presente estudio en la consolidación de conocimientos y conceptos en el tema.
La DREZ-tomía se muestra como un arma más en el arsenal de la neurocirugía funcional en el control del dolor y/o espasticidad, de alta eficacia, baja morbimortalidad y poca recurrencia. Al alcance con los recursos técnicos básicos de cualquier servicio neuroquirúrgico(62).
El éxito en los resultados está básicamente determinado por la adecuada y cuidadosa selección del paciente a ser intervenido, incluso por encima de la habilidad del cirujano y para ello se recomienda observar algunos de los criterios e indicaciones más importantes para facilitar dicha selección:
1. Pacientes con patología dolorosa o espástica que fracasaron a métodos no invasivos en el control del dolor. 2. El dolor debe tener distribución metamérica específica. 3. Mejor resultado en dolor irradiado distal que en casos de dolor axial. 4. Esperanza de vida mayor de tres meses en casos de neoplasia. 5. No debe existir factores que comprometan la cicatrización de la herida como infección, tumor adyacente o lesión por radioterapia. 6. En casos de pacientes con dolor por enfermedad maligna el procedimiento debe ser realizado en neoplasias topográficamente definidas y limitadas, porque la propagación de la enfermedad puede invadir niveles no incluidos en la DREZ-tomía con recurrencia dolorosa en regiones contiguas. De lo contrario debe considerarse la cordotomía o mielotomía comisural(1). 7. En casos de dolor intratable por avulsión de plexo braquial o lumbo-sacro y en dolor segmentario por lesión medular son las indicaciones más antiguas, con mejor resultado e internacionalmente aceptadas. El dolor posamputación y la neuralgia posherpética a parte de las presentadas en este trabajo, son posibles candidatos(24,26,62). 8. En casos de espasticidad se debe considerar el uso de la DREZ-tomía cuando esta es preferiblemente segmentaria y que mantengan funcionalidad motora residual(3).
Queda el campo abierto en Venezuela para la ampliación de los alcances de la DREZ-tomía a nivel del núcleo caudalis en dolor facial(24,26,62-64) y a nivel sacro en casos de vejiga neurogénica espástica(2).